

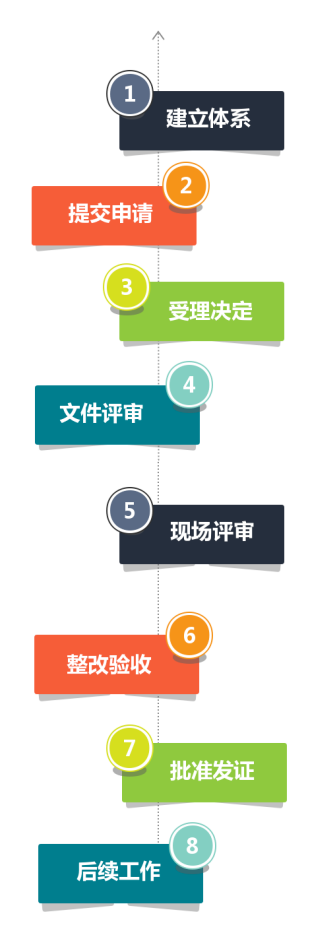
实验室若申请CNAS认可,首先要依据CNAS的认可准则,建立管理体系。医学实验室适用CNAS-CL02(等同采用ISO15189)《医学实验室质量和能力认可准则》。
1.1 实验室建立管理体系及文件。除满足基本认可准则的要求外,还要根据所开展的检测/校准/鉴定活动的技术领域,同时满足CNAS基本认可准则在相关领域应用说明、相关认可要求的规定。
1.2 实验室的管理体系至少要正式、有效运行6个月后,进行覆盖管理体系全范围和全部要素的完整的内审和管理评审。
正式运行
所谓正式运行,是指初次建立管理体系的实验室,一般要先进入试运行阶段,通过内审和管理评审,对管理体系进行调整和改进,然后再正式运行。
有效运行
所谓有效运行一般是指管理体系所涉及的要素都经过运行,且保留有相关记录。对于实验室不从事认可准则中的一种或多种活动时,如分包校准等,可按准则要求进行删减。
内审和管理评审
实验室在策划内审时,要从机构设置、岗位职责入手,从风险控制的角度确定内审范围和频次,制定内审方案。内审“检查表”(或其他称谓)要记录相应客观证据并具可追溯性。内审和管理评审方案的建立和实施可参考以下文件:CNAS-GL011《实验室和检验机构内部审核指南》、CNAS-GL012《实验室和检验机构管理评审指南》。
2
提交申请
2.1意向申请
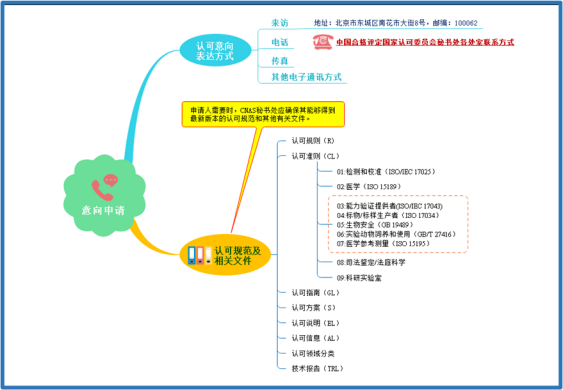
2.2 正式申请
2.2.1 实验室可登录CNAS网站“www.cnas.org.cn/“实验室/检验机构认可业务请”系统填写认可申请(CNAS-AL01、CNAS-AL02),并按申请书中的要求提供其他申请资料。
账号申请及预申请
详见在线申请账号获取说明(https://www.cnas.org.cn/zxfw/sys_jcjgrkywxt/xtbzwd/)
提交材料及缴费
详见CNAS业务管理系统--医学实验室用户手册(https://www.cnas.org.cn/zxfw/sys_jcjgrkywxt/xtbzwd/)
提交材料要求
提交纸质版材料和电子版材料的要求详见2016年6月7日CNAS发布的《关于调整实验室及相关机构、检验机构申请及评审资料提交方式的通知》。
3
受理决定
3.1 CNAS秘书处收到实验室递交的申请资料并确认交纳申请费后,首先会确认申请资料的齐全性和完整性,然后再对申请资料进行初步审查,以确认是否满足CNAS-RL01第6条所述的申请受理要求,做出是否受理的决定。
3.2 CNAS秘书处在资料审查过程中(做出受理决定前)会将所发现的问题通知申请实验室,实验室要在1个月内书面回复CNAS秘书处,对所提问题进行澄清或采取的处理措施,在回复后的2个月内,其提交的整改资料,经审查能够满足受理要求。否则会导致不予受理其认可申请的后果。注:实验室的整改有可能需要反复多次,因此实验室最好尽早提交整改材料。
3.3 由于申请人不符合申请受理条件,CNAS秘书处业务处将向申请人发出不受理认可通知书。申请人对CNAS秘书处的不受理决定有异议,可于接到不受理通知后10个工作日内,向CNAS秘书处提出申诉,逾期则视同接受CNAS对于申投诉的处理,可参看CNAS-R03《申诉、投诉和争议处理规则》。
4
文件评审
4.1 CNAS秘书处受理申请后,将安排评审组长对实验室的申请资料进行全面审查, 在文件评审中,评审组长发现文件不符合要求时,CNAS秘书处或评审组长会以书面方式通知实验室进行纠正,必要时采取纠正措施。
4.2 评审组长进行资料审查后,会向CNAS秘书处提出以下建议中的一种:
实施预评审
预评审不是预先的评审,预评审只对资料审查中发现的需要澄清的问题进行核实或做进一步了解,对预评审中发现的问题,评审组长可告知实验室,但不能提供有关咨询。预评审的结果不作为评价实验室质量管理体系和技术能力的正式依据,也不能作为减少正式评审时间的理由。
实施现场评审
文件审查符合要求,或文件资料中虽然存在的问题,但不会影响现场评审的实施时提出。
暂缓实施现场评审或不实施现场评审
文件资料中存在较多的问题,直接会影响现场评审的实施时提出,在实验室采取有效纠正措施并纠正发现的主要问题后,方可安排现场评审;
文件资料中存在较严重的问题,且无法在短期内解决时提出,或实验室的文件资料通过整改后仍存在较严重问题、或经多次修改仍不能达到要求时提出。
5
现场评审
5.1 现场评审的具体日期由CNAS秘书处或委托评审组长与实验室协商确定。
5.2 组建评审组后,由CNAS秘书处向实验室发出《现场评审计划征求意见表》征求实验室的意见, 实验室确认《现场评审计划征求意见表》后,CNAS秘书处会向实验室和评审组正式发出现场评审通知,将评审目的、评审依据、评审时间、评审范围、评审组名单及联系方式等内容通知相关方。
5.3 现场评审
首次会议
现场评审的开始以首次会议的召开为表征,首次会议由评审组长主持,评审组和实验室人员(可以是管理层人员,也可以是全体人员)参加。首次会议上评审组长将通告评审目的、范围,宣告评审要求,澄清被评审方的问题,确认评审日程,并与实验室确定陪同人员及必要的办公设施。
正式评审
现场评审时,评审组会针对实验室申请认可的技术能力进行逐项确认,根据申请范围安排现场试验。安排现场试验时会考虑申请认可的所有项目/参数、仪器设备、检测/校准/鉴定方法、类型、试验人员、试验材料等等。
在现场评审期间,评审组每天会汇总评审情况,并将当天的评审情况通告实验室。现场评审结束前评审组会将现场评审的总体情况与实验室沟通,听取实验室的意见。
末次会议
现场评审以末次会议的结束而宣告结束。
5.4 现场评审结论仅是评审组向CNAS的推荐意见,根据CNAS-J01《中国合格评定国家认可委员会章程》,由评定委员会“做出有关是否批准、扩大、缩小、暂停、撤销认可资格的决定意见。
5.5 现场评审后,实验室可登录CNAS网站服务专栏下载《实验室/检验机构评审人员评审现场状况调查表》,并于评审工作结束后5个工作日内,将填写完成的表格反馈至CNAS评审员处,对评审员现场评审表现作出评价。
6
整改验收
6.1 对于评审中发现的不符合,实验室要及时进行纠正,需要时采取纠正措施,一般情况下,CNAS要求实验室实施整改的期限是2个月。但对于监督评审(含监督+扩项评审)和复评审(含复评+扩项评审)时涉及技术能力的不符合,要求在1个月内完成整改。
6.2 部分情况下,评审组会对不符合项的整改,考虑进行现场验证,一般情况下,现场验证由原评审组进行。
6.3 评审组在现场评审结束时形成的评审结论或推荐意见,有可能根据实验室的整改情况而进行修改,但修改的内容会通报实验室。
7
批准发证
7.1 实验室通过了现场评审,并不等于获得了认可。根据CNAS-J01《中国合格评定国家认可委员会章程》规定,由评定委员会做出批准认可的决定。
7. 2 CNAS秘书处会向获准认可实验室颁发认可证书以及认可决定通知书,并在CNAS网站公布相关认可信息。实验室可在CNAS网站“获认可机构名录”中查询。注:认可批准后,CNAS将在网上预公布实验室获认可的范围,实验室如有异议可向专门信箱(scope@cnas.org.cn)发送信息,由CNAS甄别处理。
7.3 目前CNAS实验室认可周期及认可证书有效期的规定见CNAS-RL01《实验室认可规则》第5.1.7条。
8
后续工作
8.1 监督评审和复评审
8.1.1 为了证实获准认可实验室在认可有效期内能够持续地符合认可要求,CNAS会对获准认可实验室安排定期监督评审。一般情况下,在初次获得认可后的1年(12个月)内会安排1次定期监督评审,并根据实验室的具体情况(可查看CNAS-RL01《实验室认可规则》第5.3.2条),安排不定期监督评审。
8.1.2 已获准认可的实验室在认可批准后的第2年(24个月内)进行第1次复评审。复评审每2年1次,两次复评审的现场评审时间间隔不能超过2年(24个月)。复评审范围涉及认可要求的全部内容、全部已获认可的技术能力。具体要求见CNAS-RL01《实验室认可规则》第5.4条。
8.1.3 如实验室确因特殊原因不能按期接受定期监督评审或复评审,则需向CNAS秘书处提交书面延期申请,说明延期原因及延期期限,经审批后方可延期。一般情况下,延期不允许超过2个月。
8.1.4 不定期监督评审根据具体情况安排现场评审或其他评审(如文件评审)。对于获认可在6年之内的实验室,由于实验室与认可相关的人员、方法、设备、环境设施等发生变化而安排的不定期监督评审,如果这种变化导致实验室技术能力的变更或涉及的变更很多,则需要安排现场评审确认,反之可安排其他评审确认。
8.2 扩大认可范围
8.2.1 实验室获得认可后,可根据自身业务的需要,随时提出扩大认可范围申请,申请的程序和受理要求与初次申请相同,但在填写认可申请书时,可仅填写扩大认可范围的内容。扩大认可范围的相关要求请参见CNAS-RL01《实验室认可规则》第5.2.1条。
8.3 认可变更
8.3.1 实验室获得认可后,有可能会发生实验室名称、地址、组织机构、技术能力(如主要人员、认可方法、设备、环境等)等变化的情况,这些变化均要及时通报CNAS秘书处,具体要求可参见CNAS-RL01《实验室认可规则》第9条。变更发生后,实验室从CNAS网站下载并填写《变更申请书》,提交变更申请后,在CNAS秘书处确认变更前,实验室不能就变更后的内容使用认可标识。
8.3.2 针对实验室的情况,对实验室提出的认可标准、授权签字人的变更,CNAS秘书处采取不同的方式进行确认:
a) 获认可超过6年(含6年)的实验室,实施备案管理,即接到变更申请后,直接获得批准;如果实验室提出变更申请时,CNAS秘书处已确定其监督、扩项或复评评审组的,则在完成现场评审等全部认可流程后予以批准。
b) 获认可不足6年的实验室,则需要通过不定期监督评审,对申请的变更事项予以确认。
8.3.3 一般情况下,对于检测/校准/鉴定环境变化(指搬迁),需通过现场评审予以确认。
8.3.4 在认可有效期内,实验室如要缩小认可范围或不再保留认可资格,要向CNAS秘书处提交书面申请,并明确缩小认可的范围。
8.3.5 在认可有效期内,实验室如不能持续符合认可要求,CNAS将对实验室采取暂停或撤销认可的处理,具体要求可参见CNAS-RL01《实验室认可规则》第10条。被暂停认可后,实验室如要恢复认可,需书面提交恢复认可申请。暂停期内实验室如不能恢复认可(完成评审、批准环节),则将被撤销认可。