

2014年12月15日,卫生部临床检验中心发布2015年全国外周血胎儿染色体非整倍体(T21、T18和T13)高通量测序检测室间质量评价通知,表示将于2015年度正式开展全国外周血胎儿染色体非整倍体(T21、T18和T13)高通量测序检测室间质量评价。
室间质量评价也称为能力验证实验(以下简称PT),是指多家实验室分析同一标本并由外部独立机构收集、反馈实验室上报结果并评价实验室操作的活动,通过实验室间的比对判定实验室的校准、检测能力以及监控其持续能力。长期以来,PT一直是临床实验室和公共卫生实验室质量保证的一个重要组成部分。
室间质评目的:提高实验室外周血胎儿染色体非整倍体(T21、T18和T13)高通量测序检测的质量
卫生部对全国外周血胎儿染色体非整倍体(T21、T18和T13)高通量测序检测展开室间质量评价,主要目的是提高实验室外周血胎儿染色体非整倍体(T21、T18和T13)高通量测序检测的质量。通知原文如下:
“新一代高通量测序技术发展迅速,并已由实验室研究进入到临床检测应用,如外周血胎儿染色体非整倍体(T21、T18和T13)检测、胚胎植入前遗传学诊断(PGD和胚胎植入前遗传学筛查(PGS)等,其中外周血胎儿染色体非整倍体(T21、T18和T13)检测目前已有国家食品药品监督管理总局(CFDA)批准的仪器和试剂。为提高实验室外周血胎儿染色体非整倍体(T21、T18和T13)高通量测序检测的质量,卫生部临床检验中心于2015年度正式开展全国外周血胎儿染色体非整倍体(T21、T18和T13)高通量测序检测室间质量评价。”
2014室间质评结果:绝大多数结果符合预期
这并不是卫生部第一次发布全国外周血胎儿染色体非整倍体(T21、T18和T13)高通量测序检测室间质量评价通知,2014年11月,为配合卫计委新一代高通量测序技术应用试点工作,卫生部临床检验中心开展了该项目的全国室间质量评价活动,并要求各临床实验室使用日常所用试剂和程序进行检测。以下是2014室间质评主要结果,数据来源于《全国外周血胎儿染色体非整倍体(T21、T18 和 T13)高通量测序检测室间质量评价调查活动结果报告 》。
1、样本情况
本次共发放 20 个质评样本,编号分别为 1401、1402、1403、1404、1405、1406、1407、1408、1409、1410、1411、1412、1413、1414、1415、1416、1417、1418、1419、1420。样本为人血浆,样本量为 700µl。其中 15 份样本用于本次PT 成绩评价,5 份样本用于正式质评发放样本类型的参考,不纳入本次 PT 成绩评价。具体信息见下表。
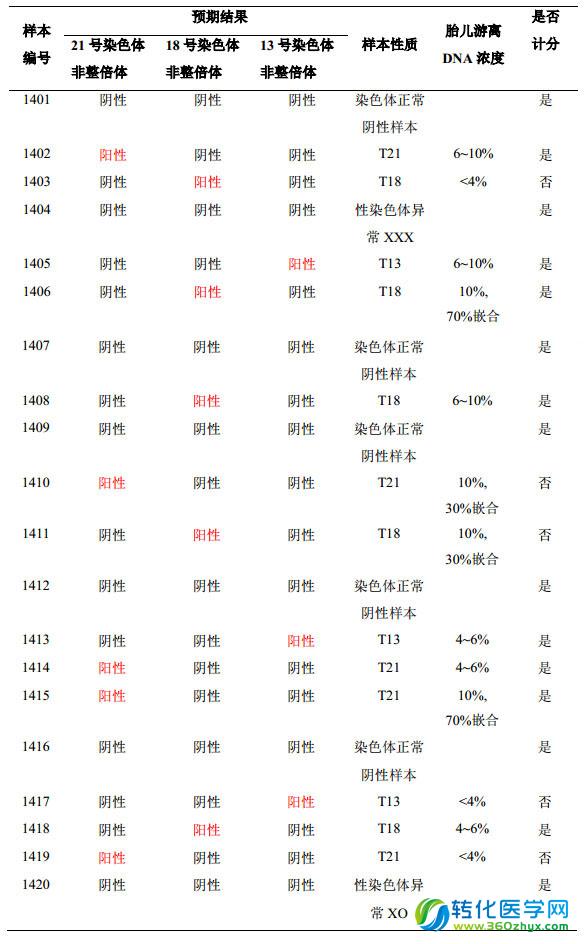
2、各检测平台使用的实验室数及相关参数
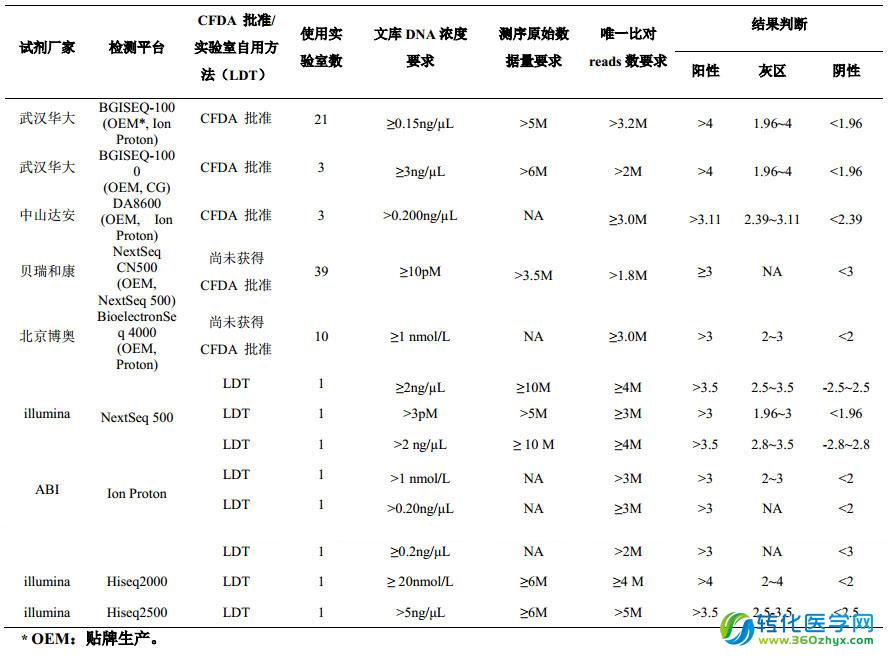
本次质评涉及多个检测平台(由于 CFDA 为检测仪器和配套试剂共同审批,因此本小结中所提及的检测平台,除 LDT 外,均同时代表该平台及相应的配套试剂)。其中有医疗器械注册证的检测平台:BGISEQ-100(武汉华大基因生物医学工程有限公司),BGISEQ-1000(武汉华大基因生物医学工程有限公司),DA8600(中山大学达安基因股份有限公司)等。其他检测平台有:NextSeq CN500,BioelectronSeq 4000,NextSeq 500,Ion Proton,Hiseq2000, Hiseq 2500,Ion torrent PGM。需要说明的是,没有医疗器械注册证的试剂和仪器,均属实验室自用方法(laboratory developed test,LDT),具体不同平台的参数见下表。
3、实验室回报结果情况
共计有 81 家实验室回报质评结果,4 家实验室报告了两个平台的检测结果,共计收到结果 85 份,其中有效结果 84 份(即回报结果完整、在截止日期内回报的结果)。医院临床实验室共计回报 73 份结果,独立实验室回报 12 份结果。总体来说,本次质评绝大多数实验室的检测结果均符合预期结果。在 15 份 PT 评价样本中,98.8% (83/84)的实验室与预期结果完全相符,只有 1 家实验室两份阳性样本报告了“临界/灰区”的结果,其余结果也均与预期结果相符,具体的总体结果回报情况见下表。
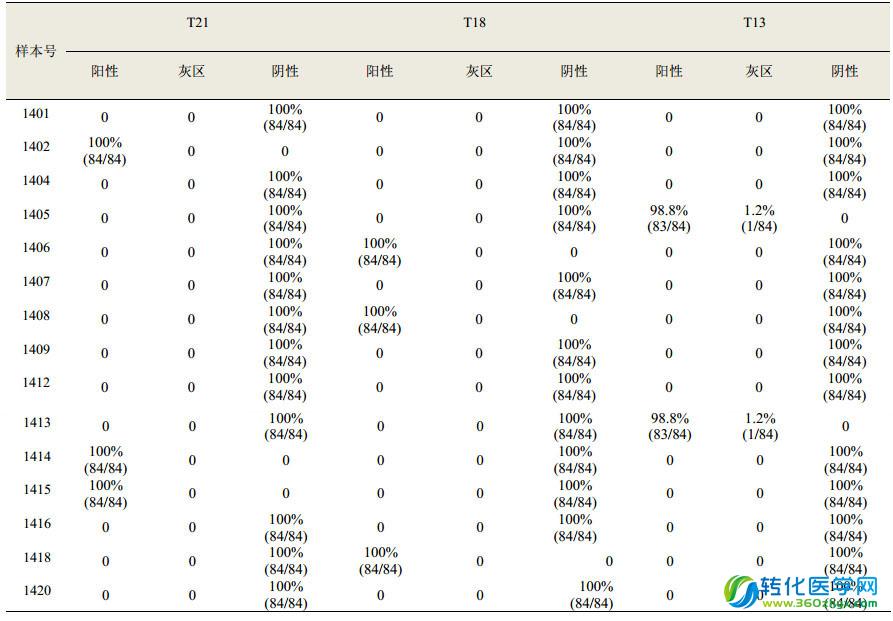
4、各检测平台不同样本的符合率情况
一家使用 Hiseq 2500 的实验室报告了 1405 和 1413 号样本(预期结果为 T13 阳性)“临界/灰区”的结果。其他平台所有实验室检测结果均与预期结果相符,无假阴性和假阳性结果。
5、各检测平台对所有样本检测的测序原始数据量和唯一比对 reads 数情况
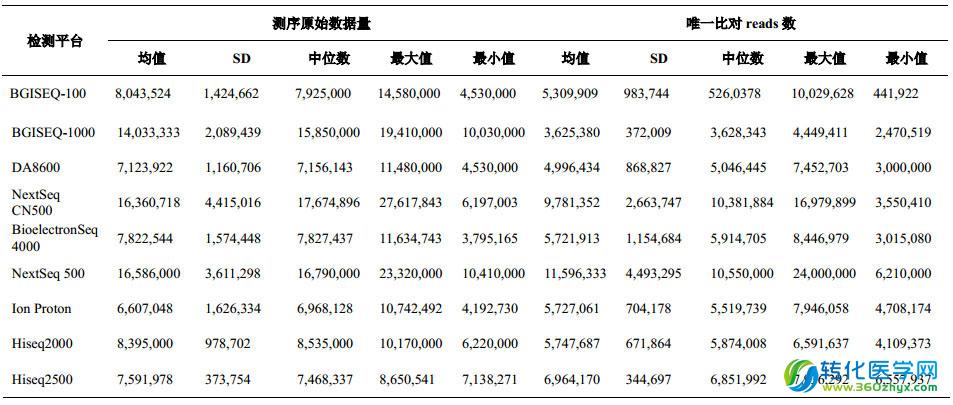
6、PT 成绩情况
PT 成绩≥80(即 80 和 100 分)的实验室发放质评合格证书;PT 成绩<80 分的实验室和未回报完整定性结果的实验室发放质评参加证书。本次质评中,PT成绩为 100 分的实验室 83 家,PT 成绩在 80~100 分(含 80 分)的实验室 1 家。1 家实验室获得质评参加证书。
对开展高通量测序 NIPT 临床检测实验室的启示
在2014室间质评的报告最后,卫计委指出:虽然各临床实验室的检测结果良好,但基于本检测项目在大多数实验室均尚未对临床开展,因此,在将来正式开展高通量测序 NIPT 临床检测中,仍需谨慎对待。
尽管目前商业化的平台(包括 CFDA 批准或正在进行注册的平台)在生物信息学分析和结果判读方面,进行了简化,但是与以往临床实验室开展的核酸检测项目相比,基于高通量测序的 NIPT 仍然是一个相对复杂的检测过程。通常,NIPT 的检测流程包括:DNA 提取,文库构建,文库纯化,文库定量,文库混合、测序以及结果分析的过程,完成一个批次的检测至少需要 3~4 天,此外,在文库构建和文库定量中,会涉及到 PCR 扩增过程。
因此,如实验室开展高通量测序 NIPT 的日常检测,需为临床基因扩增实验室,具有一定的核酸检测的基础,选择合适的检测平台,并进行性能验证,具备经过严格培训的高素质实验人员,建立实验室检测的标准操作程序,在每批次的检测中需使用阴性质控和弱阳性质控,参加室间质量评价。
具体来说,在本次质评中,部分实验室仅有两个不同的区域,不符合临床基因扩增实验室的设置要求;在选择检测平台时,医院临床实验室不建议采用实验室自用方法 (LDT),因为LDT 首先需要建立自配试剂的标准操作程序,然后还需对检测系统(包括检测仪器、试剂以及生物信息学算法)进行性能评价,给出重复性、分析敏感性、分析特异性、临床敏感性、临床特异性、阳性预测值以及阴性预测值等等性能指标,而目前来说,对于单个临床实验室,要完成 NIPT 的性能评价是非常困难的;实验室需建立标准操作程序,并需考虑到开展大量样本检测后,出现文库构建失败、检测过程操作错误、QC 未通过以及“灰区”样本需复检等情况,以及针对此情况,评价可能对检测流程和报告时间产生的影响;在当前的实验室环境条件下,仪器设备经过一定时间的运行后,是否仍能够保持良好的性能,能否保持原有的 QC未通过率以及检测失败率;此外,也不排除技术快速的发展,新的检测平台的出现,或者在原有检测平台上的进一步更新,导致现有的检测平台可能面临更新或淘汰。
临床实验室需明确,基于高通量测序的 NIPT,只是一种筛查试验,而不是诊断试验,遗传咨询和进一步的检测非常重要。并且由于检测原理是基于外周血游离 DNA,因此具有一定的检测局限性,例如母体嵌合、胎盘嵌合、双胎、外周血胎儿游离 DNA 比例低等均会对结果产生影响。
总结:无创产前检测离规范使用又近了一步
不管怎样,卫计委发布室间质评,就已预示着这项技术成熟、临床应用急需的检测离规范使用又近了一步,而2014年率先通过室间质评的技术平台,例如上文提到的华大基因、达安基因、贝瑞和康、博奥生物等公司,无疑将在后续竞争中获得合作终端和客户更多的信任。(转化医学网360zhyx.com)
附:卫生部临床检验中心2015年全国外周血胎儿染色体非整倍体(T21、T18和T13)高通量测序检测室间质量评价通知
卫检中字[2014]第04号
各参评单位实验室:
室间质量评价(以下简称“室间质评”)是临床实验室保证和改进检验质量的重要手段,也是医疗机构临床实验室行政管理和实验室认可的基本要求。新一代高通量测序技术发展迅速,并已由实验室研究进入到临床检测应用,如外周血胎儿染色体非整倍体(T21、T18和T13)检测、胚胎植入前遗传学诊断(PGD和胚胎植入前遗传学筛查(PGS)等,其中外周血胎儿染色体非整倍体(T21、T18和T13)检测目前已有国家食品药品监督管理总局(CFDA)批准的仪器和试剂。为提高实验室外周血胎儿染色体非整倍体(T21、T18和T13)高通量测序检测的质量,卫生部临床检验中心于2015年度正式开展全国外周血胎儿染色体非整倍体(T21、T18和T13)高通量测序检测室间质量评价,现将有关事项通知如下。
一、一般情况
1. 临检中心2015年外周血胎儿染色体非整倍体(T21、T18和T13)高通量测序检测室间质量评价计划相关信息见附录1。
2. 临检中心室间质评信息处理采用基于互联网的室间质评信息系统,室间质评申请、检验结果与相关信息回报、统计分析图表获取等通过信息系统完成。室间质评信息系统运行网站为检验医学信息网(http://www.clinet.com.cn),信息系统及其使用说明参见网站相关介绍。计划书内容及本通知涉及各种技术文件也可在网站获取。
3. 临检中心向参评实验室收取室间质评费用,用以维持室间质评计划运行。临检中心室间质评收费依据《国家发展改革委办公厅关于卫生部临床检验室间质量评价等收费问题的复函》(发改办价格[2003]1066号)。
二、申请
1. 2015年外周血胎儿染色体非整倍体(T21、T18和T13)高通量测序室间质量评价申请日期为自2015年1月1日至2015年1月31日,各参评实验室应在截止日期前提出申请。
2. 原参加过临检中心质评的单位直接网上申请,用本单位用户名和密码登录检验医学信息网(http://www.clinet.com.cn),完整填写“卫生部临床检验中心2015年临床检验室间质量评价申请表”(一)和(二)(见附录2);2015年新参评单位需将完整申请表(一)和(二)通过电子邮件或传真发送临检中心,发送后电话联系临检中心(联系方式见本通知第四项),以确认收到申请,同时获取实验室编码及室间质评信息系统登录信息。
3. 提交申请表后,按规定时间交纳室间质评费用。请将室间质评费用统一汇款至:
户 名:卫生部临床检验中心
开户银行:中国工商银行北京崇文门外大街支行
帐 号:0200000509014494542
联 系 人:李静
联系电话:(010)5811-5052
请务必先申请,确认申请成功后再进行汇款。
三、质控品接收、检测及统计结果和质评报告获取有关详细情况将在第一次质评样本寄出时告知。本年度质评邮寄样本的费用,采用到付的形式,即邮寄的费用由参评单位承担,特此说明。
四、联系方式
实验室遇有室间质评有关的任何问题,请与临检中心室间质评室联系,联系方式如下:
电话:(010)5811-5055、5811-5065、6527-3025
传真:(010)6527-3025
电子邮箱:EQA@nccl.org.cn
联 系 人:王薇 何法霖 钟堃 赵彦 李国华
卫生部临床检验中心
2014年12月15日